2030年に患者数130万人超―増え続ける心不全の6割を占めるタイプに新薬が承認

心機能の指標である左室駆出率による心不全の分類において、これまで治療方法が限られていた「左室駆出率40%以上の心不全」に対するエビデンスを有する非ステロイド型選択的ミネラルコルチコイド受容体拮抗薬(MRA)「フィネレノン(商品名:ケレンディア)」が2025年12月に慢性心不全の適応で追加承認されました。これを受けて、心不全はどのような病気で、どう治療されているかなどについて解説するプレスセミナー「心不全の治療が変わる、心臓のポンプ機能に着目した新たな治療戦略」(バイエル薬品主催)が2026年2月19日、東京都内で開かれました。同セミナーから、講演の内容を再構成してご紹介します。
目次 -INDEX-
心不全のメカニズムと治療法
日本の心不全患者は高齢化に伴って増え続け、2030年には130万人を超えると推計されています。心不全は、「左室駆出率(全身に血液を送り出す左心室の状態を示す指標で、一拍で心室内の血液をどれくらい送り出せるかの値)」によって、40%以下のHFrEF(左室駆出率の低下した心不全)、41~49%のHFmrEF(左室駆出率の軽度低下した心不全)、50%以上のHFpEF(左室駆出率の保たれた心不全)に分類されます。
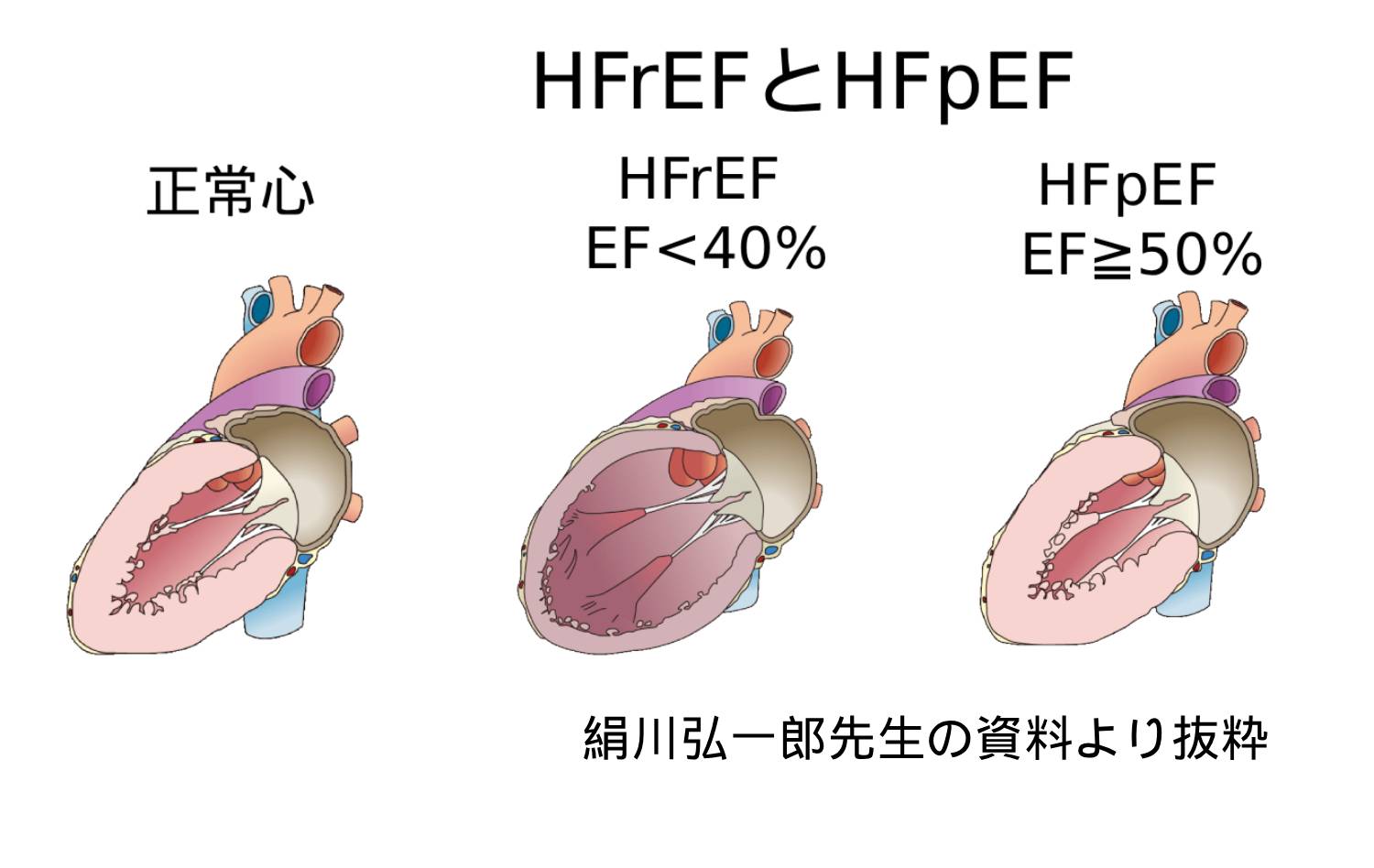
セミナーではまず、富山大学内科学第二教授の絹川弘一郎氏が「心不全診療の現状と課題:左室駆出率の保たれた心不全とは?」の演題で、HFrEFとHFpEFのメカニズムの違いや、それぞれの治療などについて解説しました。概要は以下の通りです。
死亡者数の推移―心筋梗塞が減って心不全が増える理由
心不全は心疾患による死亡者の中で最多の40%を占め、急性心筋梗塞(同16%)と並んで心疾患による二大死因の一つとされています。心不全とは単に「心臓の停止」を意味するのではなく、「心臓が悪いために、息切れやむくみがおこり、だんだん悪くなり、生命を縮める病気」と定義されています。
2000年ごろ、心不全と急性心筋梗塞の死亡者はほぼ同数でした。その後、急性心筋梗塞の死亡者は減少傾向にある一方、心不全は増加を続けています。背景として、急性心筋梗塞の発症数自体は減っていないものの救急医療が充実し、急性心筋梗塞に対するカテーテル治療(細い管を使って心臓の詰まった血管を風船やステントと呼ばれる筒状の網で広げ、血流を再開させる治療)が普及したことが死亡率を低下させています。一方、心不全は依然として予後不良で、死亡者数が増えているのです。
そのメカニズムは次のように考えられています。心臓の筋肉(以下、心筋)に血液を供給する血管が詰まることで心筋が壊死する心筋梗塞は、局所的であっても放置すると血管の詰まりがない部分の心筋にもさまざまな悪影響を及ぼし、心臓全体の動きが悪くなります。低下した心臓のポンプ機能を維持するためにレニン、アンジオテンシン、アルドステロンなど血圧を上昇させるさまざまなホルモンが分泌されます。これらのホルモンは、心筋にも直接作用します。この状態が長く続くと、心筋の病的肥大やアポトーシス(細胞が自然に死んでいくこと)、繊維化(炎症などが原因で組織が硬くなること)などが起き、心臓が拡大して収縮機能が低下し、HFrEFになります。これが心筋梗塞から心不全に至る道のりです。
交感神経の働きや、分泌されるアンジオテンシンやアルドステロンをブロックするβ遮断薬、ACE阻害薬(アンジオテンシン変換酵素阻害薬)やARB(アンジオテンシンII受容体拮抗薬)、MRAといった薬は、心不全の悪循環を抑えることで患者さんの寿命を延ばすことが期待されます。今日のテーマであるフィネレノンもMRAの一つで、これまでは2型糖尿病を合併する慢性腎臓病治療薬として使用されていました。今回、適応追加によって慢性心不全(ただし、慢性心不全の標準的な治療を受けている患者に限る)にも使えるようになりました。
薬事承認待たずガイドラインで推奨
HFrEFは心不全全体の約6割を占める中心的存在でした(2004~2005年の研究より)。ところが、2011~2015年の研究では、HFrEFは4割以下になり、代わってHFpEFが心不全全体の半数近くを占めるほどに増えてきました。心臓がどんどん大きくなるHFrEFとは全くタイプが異なり、HFpEFでは左心室が広がらなくなった結果、心臓の中の圧力が上がりやすくなり肺に血液がうっ滞する主症状がみられます。
2000年代前半から、HFrEFで効果がみられた薬がHFpEFの患者さんにも試されたのですが、ほとんどは予後改善効果に有意差がなく、長らく薬物の効果がはっきりしない時代が続いていました。ごく最近になってSGLT2阻害薬にHFpEFの予後改善効果があることがわかり、2025年3月に発行された心不全診療ガイドライン(2025年改訂版)で第一選択薬とされています。
さらに、MRAのフィネレノンが、臨床試験でHFpEFを含む左室駆出率40%以上の心不全に対する予後改善効果を示しました。MR(ミネラルコルチコイド受容体)は、心不全の増悪・進行のバックグラウンドと思われる高血圧や慢性腎臓病、肥満、糖尿病など生活習慣病で過剰に活性化されているというデータが多数あり、MRの働きを抑えることが心不全の増悪・進行に対する解決策になりうる可能性は以前から考えらえてきました。ところが、HFrEF治療に使われてきたMRAは、主要評価項目で有意なリスクの抑制を示すことはできませんでした。
フィネレノンは従来のMRAとは異なり「ステロイド骨格」という化学構造をもたないことで炎症・線維化遺伝子の発現を抑制するため、HFpEFに対する効果が期待できると考えられます。
フィネレノンの適応拡大についての薬事承認は2025年12月に出されました。従来のガイドラインは、正式に薬事承認されてから初めて載せるのが“不文律”です。しかし、ガイドラインを頻繁に改訂するわけにもいかず、臨床試験の結果もわかっていましたので、承認への高い期待を考慮し、未承認であることの注釈を入れた上で、同年3月の改訂版でHFpEFおよびHFmrEFに対して「大規模臨床試験のエビデンスの重要性を評価して、投与を考慮すべし」と推奨をしました。
国際共同治験から見えた対象患者像
続いて、フィネレノンの左室駆出率40%以上の心不全に対する効果を調べる国際共同治験「FINEARTS-HF」のナショナルリーダーを務めたかわぐち心臓呼吸器病院 循環器内科部長・副院長の佐藤直樹氏が「心不全治療はケレンディアによってどう変わるのか?」の演題で、フィネレノンの治験結果とそこから見えてきた投薬対象の患者像などについて講演しました。概要は以下の通りです。

心血管死や心不全の悪化を減少させる効果
年間50兆円を超えようとしている日本の医療費の中で、循環器系疾患が最大の約2割を占めています(「令和5<2023>年度 国民医療費の概況」)。日本循環器学会のデータによると、心不全は入院患者数、入院費用とも循環器系疾患の中で最も多く、1回の入院にかかる医療費(中央値)は100万円弱とされています。ですから、心不全の予後をよくして入院を減らすことは、医療費抑制のために非常に重要です。
FINEARTS-HF試験では、フィネレノン投与群は左室駆出率が40%以上(HFpEFとHFmrEF)の心不全患者において、心血管死およびすべての心不全イベント(初発および再発を含む心不全による入院または緊急受診)を16%減少させるという結果が得られたと報告されています。心不全はイベントを繰り返すことで徐々に心機能が低下していきますので、イベントを減らすという意味でこの薬の立ち位置は明確になっていると思います。
HFpEFと、HFmrEFの患者さんに対しては、SGLT2阻害薬が第一選択薬として強く推奨されています。ここにフィネレノンを追加するとより効果が期待できることが同治験の結果から示されています。投与にあたっては、心不全の重症度、左室駆出率、腎機能、血清カリウム濃度を基準に投与する患者さんを決めていくことになります。
使用により医療費削減につながる可能性
左室駆出率が40%以上の心不全の患者さんで予後改善が不十分なケースでは、SGLT2阻害薬が投与されていても、基準を遵守し、腎機能や血清カリウムなどのモニタリングを継続しながらフィネレノンを追加することで、イベント抑制につなぐことができればいいと思います。
心不全は、症状が落ち着いてからも慢性的に長く付き合っていく病気であるため、よい状態を保つためにも治療薬は継続して服用する必要があります。しかしながら、最初にお話ししたように心不全で入院すると1回あたり約100万円の医療費がかかることを考えると、薬によってイベント発生を抑制することは結果的に医療費の削減につながる可能性があります。
*本稿には特定の医薬品についての記述がありますが、情報提供のみを目的としたものであり、医療上の助言や販売促進などを目的とするものではありません。